نگاه اجمالی
هدف از جداسازی ، حذف مزاحمتها ، غلیظ کردن محلول مورد نظر و یا سایر موارد است. برای جداسازی از اختلاف در خصوصیات فیزیکی استفاده میشود، مثل فراریت ، حلالیت و ضریب تقسیم مواد__ و ... . در آنالیز و جداسازی مواد مختلف از تکنیکهای ویژهای برحسب نوع و ساختار مواد و مخلوطها استفاده میشود که برخی از آنها که معروف بوده و حائز اهمیت بیشتری هستند، در زیر میآوریم.تبلور
هدف از تبلور ، جداسازی ناخالصی از اجسام جامد است. در این روش ، ابتدا جامد ناخالص را در یک حلال گرم حل میکنند، سپس محلول را صاف میکنند. ناخالصیها در فاز مایع باقی میمانند. اگر تبلور طی چند مرحله صورت گیرد، به آن تبلور جزء به جزء میگویند. در این روش انتخاب حلال از اهمیت بالایی برخوردار است. اگر از تکنیک ذوب برای جداسازی ناخالصی از جامد استفاده شود، به آن تصفیه ذوب گویند.این روش در جدا کردن ناخالصیهای ژرمانیم و اسید بتروییک کاربرد دارد. در این فرآیند ، ضریب تقسیم برابر با نسبت غلظت ناخالصی در فاز جامد به غلظت ناخالصی در فاز مایع است.
تقطیر
اگر هدف از تقطیر ، جداسازی یک مخلوط به اجزای بالا باشد، از تقطیر ساده برای جداسازی اجزاء استفاده میشود. اما اگر همه اجزاء فرار باشند، از تقطیر جزء به جزء برای جداسازی استفاده میشود. اگر یک مخلوط تولید آزئوتروپ کند، ( مثل آب و الکل) نمیتوان از روش تقطیر جزء به جزء ، اجزای آن را جدا کرد. برای جداسازی این مخلوط از روشهای تقطیر با بخار آب ، تقطیر در خلاء و تقطیر ناگهانی استفاده میکنند.در تقطیر با بخار آب هیچگاه درجه حرارت تقطیر از نقطه جوش آب بیشتر نمیشود. ترکیباتی نظیر تولوئن ، اتیلن ، گلیسیرین و اسیدهای چرب از این طریق جدا میشوند. برای جلوگیری از تجزیه مایعاتی که دارای نقطه جوش بالایی هستند از تقطیر در خلاء استفاده میشود. با کاهش فشار ، نقطه جوش مایع کاهش پیدا میکند.
در تهیه آب آشامیدنی از آب دریا و تهیه آب مقطر نیروگاهها از تقطیر ناگهانی استفاده میشود. در این روش مایع بطور مداوم وارد و بخار بطور مداوم خارج میشود.
رسوب دادن
نوعی روش جداسازی است که اساس آن اختلاف حلالیت اجسام میباشد. یعنی جزیی که حلالیت کمتری دارد زودتر جدا میشود. با افزایش نیروی جاذبه سرعت تهنشین شدن افزایش پیدا میکند. عمل سانتریفوژ در واقع بر همین اساس است.استخراج
اساس این روش ، اختلاف حلالیت یک جزء در دو حلال غیر قابل حل در یکدیگر است. اگر دو حلال غیر قابل استخراج ، مایع باشند، به این روش استخراج مایع ـ مایع گویند و اگر یک جسم جامد به وسیله یک حلال استخراج شود، به آن استخراج جامد ـ مایع گویند (مثل استخراج اسانسها ، عصارهها و روغن از دانههای گیاهی). عموما دو فاز مورد استفاده ، یکی آب است و دیگری یک حلال آلی.مقداری از جسم در فاز آبی و مقداری نیز در فاز آلی میباشد. بازده استخراج با ضریب تقسیم نسبت مستقیم دارد. دوبار استخراج با حجم کمتر از حلال آلی همیشه موثر از یک بار استخراج با حجمی مساوی دو برابر حجم اول است. چون در حالت اول ، مقدار وزن ماده باقیمانده محلول در آب ، کمتر از حالت دوم خواهد بود.
کروماتوگرافی
اساس کروماتوگرافی ، جذب سطحی مواد و توزیع آنها در دو فاز میباشد. یکی از فازها ثابت و فاز دیگر متحرک است که نمونه مورد نظر در فاز متحرک جدا میشود. فاز ثابت یا جامد است و یا مایع و فاز متحرک یا مایع است و یا گاز . اگر فاز ثابت ، جامد و فاز متحرک ، مایع باشد، به آن کروماتوگرافی مایع ـ جامد ( LSC ) گویند. اگر فاز متحرک ، گاز و فاز ثابت ، جامد باشد، به آن کروماتوگرافی گاز - جامد ( GSC ) گویند. اگر فاز متحرک ، مایع و فاز ثابت نیز مایع باشد به آن کروماتوگرافی مایع ـ مایع ( LLC یا HPLC ) گویند و در نهایت اگر فاز متحرک ، گاز و فاز ثابت ، مایع باشد، به آن کروماتوگرافی گاز - مایع ( GLC یا VPC ) گویند.در LSC ، جدا شدن بر اساس جذب سطحی یا تعریض یونها و یا تشکیل کمپلکس میباشد. در GSC اساس ، جداسازی جذب سطحی است. در LLC و GLC ، مواد بر اساس توزیع بین دو فاز جدا میشوند. پس کروماتوگرافی روشی برای جداسازی مخلوط بدلیل اختلاف تحرک آنها میباشد.
کروماتوگرافی LSC در واقع نوعی کروماتوموگرافی جذبی است که مواد بر اساس اختلاف در قابلیت جذب خود روی سطح جامد از یکدیگر جدا میشوند. در GSC نیز اساس جداسازی جذب سطحی فاز گاز روی سطح جامد است. از این روش برای خالص سازی گازها استفاده میشود.
کروماتوگرافی تبادل یونی
کروماتوگرافی تبادل یونی ، روشی است که در آن ، یونها بین یک محلول و یک فاز جامد ( رزین ) مبادله میشوند. این تبادل ، برگشت پذیر است. فاز جامد در آب ، غیر محلول بوده و دارای بنیانهای اسیدی و بازی باشد. نوع معدنی این مواد جامد ، ممکن است شبیه زئولیتها باشند و نوع جدید آنها از مشتقات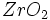 هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.
هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.تشکیل این رزینها بر اساس پلیمریزاسیون پلیاستیرن و وینیلبنزن استوار است. رزینها به دو نوع تعویض کننده آنیونی و کاتیونی تقسیم میشوند. هر کدام از این تعویض کنندهها به نوع بازی ضعیف و قوی و اسیدی ضعیف و قوی تقسیم میشوند
دید کلی
بطور کلی تمام عناصر پایدار همراه با عناصر ناپایداری که نیم عمر خیلی طویل دارند، در طبیعت یافت میشوند. لیکن از متلاشی شدن رادیواکتیوی و تکثیر ایزوتوپی ، تغییر فاحشی در وفور و فراوانی آنها پیدا میشود. میخواهیم بدانیم چه هستهها و عنصرهایی بیشتر در طبیعت وجود دارند.قاعده اودو - هارکسنیس
این قاهده عنوان میدارد که عناصری با اوزان اتمی قابل بر تقسیم بر چهار 86.5% مجموعه جرم لایه علیای لیتوسفر را تشکیل میدهد و با توجه به ساختمان و پایداری هسته اتمی عناصری که عدد اتمی آنها زوج است، باید بیش از عناصری که عدد اتمی آنها فرد است وجود داشته باشند. شاهد این مدعا همانا وجود هشت عنصر Ca , S , Mg , Si , Ni , Fe , O به میزان کلی 98.6% در سنگهای آسمانی میباشد.اما در همه جا بطور کلی صدق کرده که هر عنصر با عدد اتمی زوج ، فراوانتر از عناصر بلاواسطه طرفین خود که عدد اتمی آنها فرد است یافت میشود و بطور کلی مقدار آن بطور متوسط 70 برابر است و در حالات خاصی و استثنایی وفور و فراوانی هر عنصر با عدد اتمی زوج برابر معدل فراوانی دو عنصر بلاواسط آن میشود و شاهد این مدعا عناصری میباشند که از نظر ژئوشیمی باهم بستگی دارند، یا به عبارت دیگر باهم در طبیعت یافت میشوند که مثال بارز آن ، لانتانیدها میباشند که از لحاظ شیمیایی همگنترین گروه جدول تناوبی و از نظر ژئوشیمی بهترین دلیل اثبات قاهده "اودو - هارکنیس" میباشند.
منحنی تغییرات فراوانی عناصر لانتانید
وقتی منحنی تغییرات لانتانیدها را نسبت به عدد اتمی ، Z ، برای تمام منابع ، جو خورشید ، سنگهای آسمانی و کانیها رسم میکنیم، ملاحظه میشود که تمام نقاط ماکزیمم را عناصری که عدد اتمی Z آنها مانند Nb , Pr , Ce و غیره زوج و نقاط مینیمم را عناصر با عدد اتمی فرد مانند Eu , Pm , La و غیره است، اشغال کردهاند و جالبتر آنکه اغلب نقاط ماکزیمم و مینیمم بر روی یک خط قرار گرفتهاند، یعنی وفور آنها یکسان است.استثنای قاعده اودو - هارکینس
این قاعده نیز مانند قوانین دیگر دارای استثنا میباشد و نمیتوان آن را در همه جا صادق دانست. از جمله این استثنا فراوانی بیشتر (S(Z=16 از (P(Z=15 و یا (Mg(Z=12 از Na(Z=11) و یا (Mn(Z=25 از (Cr(Z=24 است.رابطه فراوانی عناصر با هستههای عناصر
بطور کلی فراوانی عناصر با قوانین هسته بستگی دارد و فراوانی هستههای پایدار که بحث مفصل آن به فیزیک هسته بیشتر مربوط میشود، تابع سه عامل قرار میگیرد؛ یکی انرژی پیوندی هسته یا انرژی غلاف بندی هسته و دیگری به عدد جرم A یعنی مجموع پروتونها و نوترونهای هسته ، زیادتی و مازاد نوترونها. منظور از انرژی پیوند هسته این است که معلوم داریم چگونه ذرات نوترون و پروتون ، اگر هسته را محض سهولت فهم متشکل از این دو ذره بدانیم، در درون هسته به هم پیوستهاند.بر اساس تئوری نوترون و پروتون هسته اتمی ، هر هسته دوترون ، شامل یک نوترون و یک پروتون است. وقتی به مقایسه جرم یک پروتون آزاد و یک نوترون آزاد با جرم یک دوترون که از اتحاد آنها بدست آمده است، میپردازیم ملاحظه میشود که مجموع جرم پروتون و نوترون برابر با 2.01712 است و حال آنکه جرم دوترون برابر با H = 2.01474 میباشد این اختلاف جرم 0.00238 بر حسب واحد جرم اتمی amu ناشی از سنجش غیر دقیق جرم نیست، بلکه به سبب اتلاف انرژی است که بکار رفته تا این دو ذره را به هم پیوند دهد.
محاسبه فراوانی بر حسب عدد نوترون N
اولین محاسبه ایزوتوپها در 1937 توسط "گلدشمیت" انجام گرفت که منحنی آن قابل رسم و تفسیر است و به همان نظم و ترتیبی که در سایر منحنیها مشاهده میشود، برخورد میکنیم.محاسبه فراوانی از روی عدد جرم
در 1937، "گلدشیمت" به محاسبه جمع مقادیر ایزوبارها پرداخت و از روی آن توانست منحنی تغییرات (Log S = f(A را رسم کند که S ، مقدار وفور را نشان میدهد.- فراوانی هستهها با عدد جرم فرد با جرم عناصر منظما تغییر میپذیرد و هستهها که در مجاورت خود ایزوبار دارند، از این قاعده مستثنا هستند. مانند Os , Te , Sn , Sr . در این حالات وقتی دو ایزوبار با یک عدد جرم A وجود دارند، جمع فراوانی ایزوبارها منظما تغییر میپذیرد.
- فراوانی هستهها با عدد جرم زوج و با اختلاف مشابه و مساوی نوترونها یعنی N - Z منظما با جرم تغییر میپذیرد. وقتی به رسم تغییرات در سه بعد (N , Z , Log S) میپردازیم، ملاحظه میشود که فراوانی تمام هستهها که عدد جرم آنها زوج است بر روی یک سطح منحنی قرار میگیرند، اما برای این قاعده هم موارد استثنایی وجود دارد.
- برای هستههای متوسط و سنگین که عدد جرم آنها فرد و یا زوج میباشد میتوان قاعده زیر را بیان داشت. برای عدد جرم ایزوباری که اختلاف نوترونی آن پایینتر است، فراوانی کمتر است. A=70 چهار مورد استثنایی 142 , 116 ,110 , 76 پیدا شده است.
نتایج بررسیها
با توجه به قواعد فراوانی مذکور در فوق که با حقایق فیزیکی هسته وفق میدهد. "سوئس" موفق شد که به محاسبه مجدد فراوانی کهکشانی عناصر متوسط و سنگین بپردازد و مقادیری را که "گلدشیمیت" برای لانتانیدها محاسبه کرده بود پایه و اساس قرار دهد. مقادیر حاصله کاملا با حقایقی که در مورد ساختمان ایزوتوپی عناصر کشف شده بود وفق میداد. بر حسب "سوئس" ، مقادیر جدید فراوانی معلوم میدارد که عناصر زیر در سنگهای آسمانی نسبت به سایر منابع کهکشانی وجود ندارد و یا به مقدار خیلی ناچیز وجود دارند.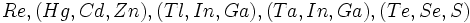
باید توجه داشت که این سه دسته عناصر از نظر شیمیایی و آرایش الکترونی مشابه میباشند و فقدان آنها سبب واکنشهای ثانویه دیگری است. مقادیر جدید وفور که از روی منحنی نمایش آنها داده میشود، بخوبی عنوان میدارد که بعضی هستهها که عدد اتمی Z (عدد پروتونی) و عدد نوترونی N معین و مشخص دارند، تفوق حاصل نمودهاند. چنانچه هستههایی که N آنها 82 , 50 , 28 , 20 و Z آنها 82 , 74 , 50, 28 است، در کهکشانها فراوان میباشند. به همین ترتیب هستههایی که زیادتی نوترون آنها 26 , 24 , 12 , 4 است از سایر هستهها فراوانترند
تعریف گالوانومتر:
بسته به مقدار جریان اثرهای آن به میزان متفاوت بروز می کنند. بنابر این برای اندازه گیری جریان می توان از هر یک از اثرهای شیمیای ، گرمایی یا مغناطیسی آن استفاده کرد وسایلی که برای اندازه گیری جریان به کار می روند، گالوانومتر نامیده می شود.
گالوانومتر ساده:
ساده ترین نوع گالوانومتر با استفاده از اثر گرمایی جریان ساخته شده است. این گالوانومتر دارای دو سیم نازک است که یکی از سیم ها در دو انتهایش ثابتند. و جریان گذرنده از آن اندازه گیری می شود. سیم نازک و محکم دوم دور محور عقربه پیچیده شده است. وسط سیم کشیده اول را به فنر کشیده ای وصل می کنند که سر دیگرش به بدنه گالوانومتر متصل است.
بر اثر جریان ، سیم اول گرم و دراز می شود. رشته سیم که توسط فنر کشیده می شود عقربه گالوانومتر را به اندازه زاویه معینی می چرخاند که بستگی به دراز شدن سیم یعنی شدت جریان الکتریکی دارد. صفحه گالوانومتر برای جریان بر حسب آمپر ، میلی آمپر مدرج می شود. در این صورت گالوانومتر آمپرسنج یا میلی آمپر سنج نامیده می شود.
آمپرسنج برای اندازه گیری جریان:
برای اندازه گیری جریان گالوانومتر یا آمپرسنج باید طوری اتصال داده شود که جریان کل مدار بتواند از آن عبور کند. برای این منظور باید در نقطه ای مدار را قطع و دو انتهایش را به قطب آمپر سنج وصل کرد. به عبارت دیگر آمپرسنج را باید به طوری متوالی در مدار قرار داد. چون جریان حالت ثابت را اندازه می گیریم. اینکه وسیله را به کدام قسمت از مدار وصل کنیم اهمیتی ندارد در صورتیکه در جریانهای متغییر چنین نیست.
ولت سنج برای اندازه گیری ولتاژ:
با استفاده از گالوانومتر نه فقط جریان بلکه ولتاژ را نیز می توان اندازه گرفت. زیرا بنابر قانون اهم این کمیت ها متناسبند. اگر دو کمیت با یکدیگر متناسب باشند با وسیله ای که به طور مناسب مندرج شده باشد می توان هر دو کمیت را اندازه گرفت. مثلاً تاکسی متر که فاصله طی شده را اندازه می گیرد، می توان برحسب کیلومتر مدرج کرد. ولی چون کرایه با فاصله متناسب است، درجات شمارنده را بطور مستقیم به پول پرداختی مدرج می کنند. به طوری که مستقیماً کرایه را نشان می دهد.
به همین ترتیب صفحه گالوانومتر را می توان طوری مدرج کرد که بتواند بطور مستقیم هم جریان برحسب آمپر عبور کرده از وسیله و هم ولتاژ دو سر آن را برحسب ولت اندازه بگیرد. بنابر این گالوانومتری که برای جریان مدرج می شود آمپرسنج ، در حالی که وسیله ای که برای ولتاژ مدرج می شود و لت سنج نام دارد.
دستگاه ها ی مرکب:
در حالت کلی اگر جریان I از گالوانومتر عبور کند، باید بین قطب های ورودی و خروجی آن ولتاژ معین U وجود داشته باشد. فرض کنید که مقاومت داخلی گالوانومتر یعنی مقاومت قسمت هایی از آن که جریان از آنها عبور می کند، R باشد (برای گالوانومتر ها با مغناطیس دائمی R مجموع تاب و سیم های رابط است، در حالی که برای گالوانومترهای با سیم افروزشی R مجموع مقاومت سیم گرم شده و رابط هاست).
بنابر قانون اهم U=IR می باشد. پس برای یک گالوانومتر معین ، هر مقدار از جریان با مقدار معینی از ولتاژ در دو سر قطب های آن متناظر است. بنابر این جای قرار گرفتن عقربه می تواند هم جریان و هم ولتاژ را نشان دهد. یعنی دستگاه را می توان هم به عنوان آمپرسنج و هم به عنوان ولت سنج مدرج کرد.
چگونگی قراردادن ولت سنج در مدار:
با استفاده از یک ولت سنج مدرج می توان اختلاف پتاسیل الکتریکی بین هر دو نقطه از مدار را اندازه گرفت. مثلا اگر اختلاف پتاسیل دو سر یک لامپ رشته ای را که از چشمه جریانی تغذیه می کند بخواهید اندازه گیری کنید. باید دو سر ولت سنج را به دو سر لامپ ببندید. به عبارتی ولت سنج جهت سنجش اختلاف پتاسیل (ولتاژ) دو نقطه از مدار یا یک عنصری از مدار بصورت موازی در مداز گذاشته می شود.
به عبارتی ولتاژ گذرنده از ولت سنج همان ولتاژ تمامی قسمت هایی از مدار است که آرایش موازی با ولت سنج دارد. در صورتیکه در مورد آمپر سنج قرارگیری در مدار بصورت متوالی است. و با اندازه گیری جریان گذرنده از یک تکه از مدار جریان کل مدار را می دهد، که باید با جریان المان مداری اندازه گیری شده ، برابر باشد.
مقاومت درونی ولت سنج:
ولت سنج را به جزئی از مدار که ولتاژ دو سر آن باید اندازه گیری شود به طور موازی می بندند. و از این رو جریان معینی ازمدار اصلی از آن می گذرد. پس ازاینکه ولت سنج وصل شد، جریان و ولتاژ درمدار اصلی قدری تغییر می کند. به طوری که حالا مداری متفاوت از رساناها داریم، که شامل رساناهای قبلی و ولت سنج است. مثلا با اتصال ولت سنج با مقاومت Rv به طوری موازی با لامپی که مقاومتش Rb است مقاومت کل مدار بصورت
(R= Rb/(1+Rb/Rv خواهد بود. هر چه مقاومت ولت سنج در مقایسه با مقاومت لامپ بزرگتر باشد، اختلاف بین مقاومت ولت سنج باید تا حد امکان بزرگ اختیار شود. برای این منظور یک مقاومت اضافی را که ممکن است مقاومتش به چند هزار اهم برسد، گاهی به طور متوالی به قسمت اندازه گیر ولت سنج می بندند.
مقاومت درونی آمپرسنج:
برخلاف ولت سنج، آمپرسنج همیشه در مدار به طور متوالی بسته می شود اگر مقاومت آمپرسنج Ra و مقاومت مدار Rc باشد، مقاومت کل مدار با آمپرسنج برابر می شود با :
(R=Rc(1+Ra/Rc
بنابر این در صورتیکه مقاومت وسیله در مقایسه با مقاومت مدار کوچک باشد بر طبق رابطه اخیر وسیله مقاومت کل مدار را زیاد تغییر نمی دهند. بنابر این مقاومت آمپرسنج ها را خیلی کوچک انتخاب می کنند (چنددهم یاچندصدم اهم).
نقش شیمی تجزیه در علوم
شیمی تجزیه نقش حیاتی در توسعه علوم دارد. به عنوان مثال ، "ویلهلم اسوالد" (Wilhelm Ostwald) در سال 1894 نوشت:««شیمی تجزیه یا هنر تشخیص مواد مختلف و تعیین اجزای سازنده آن ، نقش اول را در کاربردهای مختلف علوم دارد؛ چرا که پاسخگوی سوالاتی است که در هنگام اجرای فرایندهای شیمیایی برای مقاصد علمی و فنی مطرح میشود. اهمیت فوقالعاده آن ، باعث شده است که از همان دوران نخستین تاریخ شیمی ، مجدانه شروع به رشد و توسعه کند و سوابق موجود شامل بخش قابل ملاحظه ای از کارهای کمی است که تمامی علوم را در بر میگیرد".»»
از زمان اسوالد تاکنون ، شیمی تجزیه از یک هنر به یک علم در زمینههای مختلف صنعت ، طب و سایر علوم ، تحول و تکامل یافته است. بهعنوان مثال :
- برای تعیین کارآیی وسایل کنترل دور ، لازم است مقدار هیدروکربنها ، اکسیدهای نیتروژن و منوکسید کربن موجود در گازهای اگزوز اتومبیل اندازه گیری شوند.
- اندازه گیری کمّی کلسیم یونیده در سرم خون ، ما را در تشخیص مرض پاراتیروئید در بیماران یاری میکند.
- با اندازه گیری کمی نیتروژن در مواد غذایی ، میزان پروتئین موجود در آنها و در نتیجه ارزش غذایی آنها معلوم میشود.
- مقدار مرکاپتان موجود در گازهای مصرفی خانهها بطور مستمر تحت کنترل قرار میگیرد تا از وجود مقدار معینی مرکاپتان برای ایجاد بوی نامطبوع که هشدار دهنده نشت گاز است، اطمینان حاصل کنند.
- کشاورزان متجدد ، کود شیمیایی و آبیاری را به نحوی تنظیم میکنند که منطبق با نیاز گیاه در طی فصلهای رشد باشد. آنها این نیاز را از تجزیه کمی گیاه و خاکی که گیاه در آن میروید، معلوم میکنند.
- اندازه گیریهای کمی دارای نقش حیاتی در بسیاری از کارهای پژوهشی در زمینههای شیمی ، زیست شناسی ، زیست شیمی ، زمین شناسی و سایر علوم است.
طبقهبندی روشهای تجزیه کمی
نتایج یک تجزیه کمی را از دو اندازه گیری بدست میآوریم. یکی وزن یا حجم نمونه مورد اندازه گیری است و دوم ، اندازه گیری کمیتی است که با مقدار ماده مورد تجزیه در آن نمونه متناسب میباشد. معمولا در مرحله دوم ، تجزیه ، کامل میشود. شیمیدانان روشهای تجزیه را بر طبق طبیعت این اندازه گیری اخیر طبقهبندی میکنند. در یک روش وزنی ، جرم آنالیت یا جرم مادهای که بطور شیمیایی به آن ارتباط دارد، تعیین میشود. در یک روش حجمی ، حجم محلولی که دارای مقدار کافی واکنشگر برای واکنش کامل با آنالیت است، اندازه گیری میشود.روشهای الکتروشیمیایی شامل اندازه گیری خواصی نظیر پتانسیل ، جریان ، مقاومت و مقدار الکتریسیته است. روشهای طیفبینی بر مبنای اندازه گیری برهمکنش بین تابش الکترومغناطیسی و اتمها یا مولکولهای آنالیت (اثر تابش بر ماده) و یا تولید چنین تابشی توسط آنالیت استوارند.
بالاخره ، باید به چند روش متفرقه نیز اشاره کرد. این روشها شامل اندازه گیری خواصی چون نسبت جرم به بار ( طیف سنجی جرمی ) ، سرعت واپاشی پرتوزایی ، گرمای واکنش ، رسانندگی گرمایی ، فعالیت نوری و ضریب شکست است.
انتخاب روش تجزیه
اولین مرحله حیاتی در هر تجزیه کمی ، انتخاب روش است. انتخاب گاهی دشوار است و به تجربه و بصیرت شیمیدان بستگی دارد. از عوامل مهم در انتخاب روش ، میزان صحت مورد انتظار است. متاسفانه برای دستیابی به نتایج بسیار مطمئن ، همواره لازم است که وقت زیادی نیز صرف شود. معمولا ، روش را بر اساس مصالحه بین میزان صحت و جنبههای اقتصادی انتخاب میکنند.دومین عاملی که در ارتباط با جنبههای اقتصادی در نظر گرفته میشود، تعداد نمونههای مورد تجزیه است. اگر تعداد نمونهها زیاد باشد، در آن صورت میتوان وقت زیادی را صرف عملیات مقدماتی نظیر نصب و درجهبندی دستگاهها و وسایل و همچنین تهیه محلولهای استاندارد کرد، اما اگر فقط یک نمونه یا نهایتا تعداد کمی نمونه داشته باشیم، شاید صلاح در انتخاب روشی باشد که مراحل مقدماتی را یا نداشته و یا حداقل ممکن را داشته باشد.
نمونه برداری
برای دستیابی به اطلاعات ارزشمند ، لازم است تجزیه بر روی نمونه ای انجام شود که ترکیب آن ، کاملا معرف تمامی مادهای که نمونه از آن انتخاب شده است، باشد. هنگامی که ماده بزرگ و ناهمگن است، برای انتخاب نمونه نماینده باید سعی و دقت بسیار معطوف شود. نمونه برداری چه ساده باشد، چه پیچیده ، شیمیدان قبل از آغاز عملیات تجزیه باید از اینکه نمونه آزمایشگاهی نماینده کل محموله است، اطمینان یابد.تهیه نمونه آزمایشگاهی
یک نمونه جامد آزمایشگاهی را آسیاب میکنند تا اندازه ذرات آن کاهش یابد، سپس مخلوط میکنند تا همگن شود و قبل از انجام تجزیه بر روی آن ، برای مدت زمانهای مختلف نگهداری میکنند. در هر یک از این مراحل ، برحسب میزان رطوبت محیط ، ممکن است جذب یا دفع سطحی آب اتفاق افتد. چون ممکن است جذب یا دفع آب باعث تغییرات شیمیایی در نمونه شود، لذا بهتر است نمونهها را درست قبل از انجام تجزیه ، خشک کنیم. روش دیگر آنکه ، رطوبت نمونه را همزمان با انجام تجزیه بر روی نمونه ، طبق یک روش جداگانه ، اندازه گیری کنیم.استفاده از نمونههای همتا
اکثر تجزیههای شیمیایی بر روی نمونههای همتا که وزن یا حجم آنها با دقت توسط ترازوی تجزیه و یا یک وسیله حجمی دقیق تعیین شده است، انجام میشود. همتاسازی موجب ارتقای کیفیت نتایج و همچنین معیاری برای قابلیت اطمینان آنها خواهد بود.تهیه محلولهای نمونه
بیشتر تجزیهها بر روی محلول حاصل از نمونهها انجام میشود. در حالت ایدهآل ، حلال باید تمامی نمونه (نه فقط آنالیت) را بهسرعت و بطور کامل حل کند. شرایط انحلال باید در حد امکان ملایم باشد تا مانع از اتلاف آنالیت شود. متاسفانه بسیاری از مواد مورد تجزیه در حلالهای معمولی نامحلولند. مواد سیلیکاتی ، بسپارهای با جرم زیاد یا نسوج حیوانی از این قبیل هستند. در چنین مواردی تبدیل آنالیت به حالت محلول میتواند یک امر دشوار و وقتگیر باشد.حذف تداخل کنندهها
تعداد کمی از خواص شیمیایی و فیزیکی مهم در تجزیههای شیمیایی به گونه شیمیایی خاصی منحصر است. در عوض ، واکنشهایی که بکار میرود و خواصی که اندازه گیری میشود، شامل ویژگی گروهی از عناصر و ترکیبات است. گونههای غیر از آنالیت را که بر اندازه گیری نهایی موثرند، «تداخل کننده» مینامند. تدابیری باید اندیشید تا قبل از اندازه گیری نهایی ، آنالیت از تداخل کنندهها جدا شود. هیچ قاعده و قانون قطعی برای حذف تداخل کنندهها نمیتوان ذکر کرد که حل این مساله ، دشوارترین مرحله یک تجزیه است.درجهبندی و اندازه گیری
تمامی نتایج حاصل از تجزیه به اندازه گیری نهایی X که یک خاصیت فیزیکی آنالیت است، بستگی دارد. این خاصیت باید به صورت معین و تکرارپذیر با تغییر غلظت آنالیت CA تغییر کند. در حالت ایدهآل ، خاصیت فیزیکی اندازه گیری شده ، مستقیما با غلظت متناسب است. یعنی :که در آن k ثابت تناسب است. برای روشهای تجزیه ، باید مقدار k به صورت تجربی و با CA معلوم تعیین شود. فرایند تعیین مقدار k مرحله مهمی است و به نام درجهبندی موسوم است.
محاسبه نتایج
معمولا ، محاسبه غلظت آنالیت با استفاده از دادههای تجربی ، بویژه با ماشینهای محاسبه و کامپیوتر مدرن ، یک امر ساده و سرراست است. چنین محاسباتی بر مبنای دادههای خام که در مرحله اندازه گیری بدست آمدهاند و همچنین استوکیومتری واکنش شیمیایی که تجزیه بر اساس آن انجام یافته است و بالاخره عوامل دستگاه ، استوار است.ارزیابی نتایج و برآورد میزان اطمینان آنها
نتایج تجزیه بدون برآورد میزان اطمینان آنها کامل نیست. شخص آزمایش کننده ، برای آنکه دادهها ارزشمند باشند، لازم است میزان عدم قطعیت نتایج محاسبه شده را معلوم کند (محاسبه خطا).شیمی تجزیه نقش حیاتی را در توسعه علوم مختلف به عهده دارد، لذا ابداع فنون جدید تجزیه و بسط و تکامل روشهای تجزیه شیمیایی موجود، آنقدر سریع و گسترده است که اندکی درنگ در تعقیب رویدادهای تازه سبب بوجود آمدن فاصلههای بسیار زیاد علمی خواهد شد. نقش این فنون در فعالیتهای تولیدی روز به روز گستردهتر و پردامنهتر میگردد. امروزه کنترل کیفیت محصولات صنعتی و غیر صنعتی، جایگاه ویژهای دارد که اساس این کنترل کیفیت را تجزیههای شیمیایی انجام شده به کمک روشهای مختلف تجزیهای تشکیل میدهد.
سیر تحولی و رشد
اصولا توسعه و تغییر پایدار در فنون و روشهای تجزیه وجود دارد. طراحی دستگاه بهتر و فهم کامل مکانیسم فرآیندهای تجزیهای، موجب بهبود پایدار حساسیت، دقت و صحت روشهای تجزیهای میشوند .چنین تغییراتی به انجام تجزیههای اقتصادیتر کمک میکند که غالبا به حذف مراحل جداسازی وقت گیر، منجر میشوند. باید توجه داشت که اگر چه روشهای جدید تیتراسیون مانند کریوسکوپی، Pressuremetriz ، روشهای اکسیداسیون_احیایی و استفاده از الکترود حساس فلوئورید ابداع شدهاند، هنوز از روشهای تجزیه وزنی و تجزیه جسمی (راسب کردن، تیتراسیون و استخراج بوسیله حلال) برای آزمایشهای عادی استفاده میشود .به هر حال در چند دهه اخیر، تکنیکهای سریعتر و دقیقترِی بوجود آمدهاند. در میان این روشها میتوان به اسپکتروسکوپی ماده قرمز، ماورای بنفش و اشعه X اشاره کرد که از آنها برای تشخیص و تعیین مقدار یک عنصر فلزی با استفاده از خطوط طیفی جذبی یا نشری استفاده میگردد. سایر روشها عبارتند از:
?انواع کروماتوگرافی که به توسط آنها اجزای یک مخلوط گازی بوسیله آن از درون ستونی از مواد متخلل یا از روی لایههای نازک جامدات پودری تعیین میگردند.
?تفکیکی محلولها در ستونهای تبادل یونی
?آنالیز عنصر ردیاب رادیواکتیو.
?ضمنا میکروسکوپی الکترونی و اپتیکی، اسپکترومتری جرمی، میکروآنالیز، طیفسنجی رزونانس مغناطیسی هستهای (NMR) و رزونانس چهار قطبی هسته نیز در همین بخش طبقه بندی میشوند.
خودکارسازی روشهای تجزیهای در برخی موارد با استفاده از رباتهای آزمایشگاهی، اهمیت روزافزونی پیدا کرده است. چنین شیوهای، انجام یکسری تجزیهها را با سرعت، کارایی و دقت بهتر امکانپذیر میسازد. میکروکامپیوترها با قابلیت شگفتانگیز نگهداری دادهها و بستههای نرم افزار گرافیکی بطور قابل ملاحظهای موجبات جمع آوری، نگهداری، پردازش، تقوبت و تفسیر دادههای تجزیهای را فراهم میآورند.
انواع تجزیه
وقتی آزمایش به شناسایی یک یا چند چیز جز از یک نمونه (شناسایی مواد) محدود میگردد، تجزیه کیفی نامیده میشود، در حالی که اگر آزمایش به تعیین مقدار یک گونه خاص موجود در نمونه (تعیین درصد ترکیب در مخلوطها یا اجزای ساختمانی یک ماده خالص) محدود گردد، تجزیه کمی نامیده میشود.گاهی کسب اطلاعاتی در زمینه آرایش فضایی اتمها در یک مولکول یا ترکیب بلورین ضروری است، یا تاکید حضور یا موقعیت برخی گروههای عامل آلی در یک ترکیب مورد تقاضا است، چنین آزمایشهایی تحت عنوان تجزیه ساختمانی نامیده میشوند و ممکن است با جزئیاتی بیش از یک تجزیه ساده مورد توجه قرار گیرند.
ماهیت روشهای تجزیه ای
روشهای تجزیهای معمولا به دو دسته کلاسیک و دستگاهی طبقه بندی میشوند. روشهای کلاسیک شامل روشهای شیمیایی مرطوب، نظیر وزن سنجی و عیار سنجی است. در واقع تفاوت اساسی بین روشهای دو دسته وجود ندارد. همه آنها مشتمل بر وابستگی یک اندازه گیری فیزیکی به غلظت آنالیت میباشند. در حقیقت روشهای تجزیهای محدودی وجود دارند که صرفا دستگاهیاند و یا بیشتر آنها متضمن مراحل شیمیایی متعددی قبل از انجام اندازه گیری دستگاهی هستند.
?کنترل کیفیت محصول
بیشتر صنایع تولیدی نیازمند به تولید با کیفیت یکنواخت هستند. برای کسب اطمینان از برآورده شدن این نیازمندی مواد اولیه و همچنین محصول نهایی تولید، مورد تجزیههای شیمیایی وسیعی قرار میگیرند.
?نمایش و کنترل آلوده کنندهها
فلزات سنگین پسماندههای صنعتی و حشره کشهای آلی کلردار ، دو مشکل کاملا شناخته شده مربوط به ایجاد آلودگی هستند. به منظور ارزیابی چگونگی توزیع و عیار یک آلوده کننده در محیط، به یک روش تجزیهای حساس و صحیح نیاز است و در کنترل پسابهای صنعتی، تجزیه شیمیایی روزمره حائز اهمیت است.
?مطالعات پزشکی و بالینی
عیار عناصر و ترکیبات مختلف در مایعات بدن، شاخصهای مهمی از بی نظمیهای فیزیولوژیکی میباشند. محتوی قند بالا در ادرار که نشانهای از یک حالت دیابتی است و وجود سرب در خون، از شناختهترین مثالها در این زمینه میباشد.
?عیارگیری
از دیدگاه تجارتی در برخورد با مواد خام نظیر سنگهای معدنی، ارزش سنگ معدن، از روی فلز موجود در آن تعیین میشود. این موضوع، مواد با عیار بالا را نیز غالبا شامل میشود. بطوری که حتی تفاوت کم در غلظت میتواند از نظر تجاری تاثیر قابل ملاحظهای داشته باشد. بنابراین یک روش تجزیهای قابل اعتماد و صحیح از اهمیت اساسی برخوردار است.
?آینده شیمی تجزیه بروز مشکلات تجزیهای در شکلهای جدیدش ادامه دارد. میزان تقاضای مربوط به انجام تجزیه در ابعاد وسیع توسط بسترهای دستگاهی بطور مداوم در حال افزایش است. کاوشهای فضایی، نمونههای گمانه زنی و مطالعات اعماق دریاها مثالهایی از نیازهای قابل طرح میباشند. در دیگر زمینهها نظیر مطالعات محیطی و بالینی، فرم شیمیایی و دقیق یک عنصر در یک نمونه و نه غلظت کلی آن، اهمیت فزایندهای پیدا کرده است. دو مثال کاملا شناخته شده در این زمینه، میزان سمیت بسیار زیاد ترکیبات آلی جیوه و سرب در مقایسه با ترکیبات مشابه معدنی است.
اطلاعات اولیه
یکی از خصوصیات اساسی کروماتوگرافی این است که مخلوط اجسام ابتدا بصورت یک نوار در ستون که در نتیجه جذب سطحی یا جذب بوسیله فاز ساکن بوجود میآید، ظاهر میشود. برای جداسازی مواد ، اجزا باید عمل دیگری روی نوار به یکی از سه روش انجام میگیرد. عمده روشهای جداسازی مواد اجزاء در زیر بررسی میشود.تجزیه به روش شستشو با حلال خالص
این روش در کروماتوگرافی تقسیمی بکار میرود. در روش شستشو ، جریان فاز متحرک (محلول شستشو) را تا جداسازی مواد کامل اجزای مخلوط ادامه میدهند. جریان مایع را آنقدر از ستون ادامه میدهند که هر جزء بطور کامل از ستون خارج شود و سپس آنرا در محلول خارج شده از ستون بوسیله آزمایشهای فیزیکی یا شیمیایی مناسب تشخیص میدهند.در روش شستشوی مرحلهای از عوامل شوینده متعدد بطور متوالی استفاده میشود. این محلولها طوری مرتب شدهاند که هر یک از آنها ، در خارج کردن یک جسم معین از ستون ، از محلول قبلی مؤثرتر باشد.
روش دیگر که تجزیه شستشوی تدریجی نامیده میشود. در کروماتوگرافی جذب سطحی (از جمله تبادل یونی) اهمیت زیادی دارد. این روش همچنین در کروماتوگرافی مایع-مایع ، وقتی که حرکت نوارها بکندی انجام میگیرد، بکار میرود. در این روش از یک عامل شوینده قویتر از شویندههای معمولی استفاده میشود. محلول را طوری به ستون اضافه میکنند که یک شیب پیوسته غلظتی در ستون بوجود آید.
در این صورت قسمت عقب هر نوار کروماتوگرافی همیشه بیشتر از قسمت جلویی آن در تماس با محلول شوینده قویتر قرار میگیرد و هر نوار در محیط شوینده قویتر نسبت به نوار جلویی قرار میگیرد. بدین ترتیب ، اثر حاصل به دو گونه بروز میکند، هر نوار در ناحیه باریکتری از ستون فشرده شده و فاصله بین نوارها کاسته میشود.
تجزیه جبههای
در این روش ، محلولی از یک مخلوط بطور پیوسته ، تا اشباع شدن ستون ، افزوده میشود. این روش مخصوصا در کروماتوگرافی جذب سطحی مناسب است. البته جداسازی مواد کامل بوسیله این روش ممکن نیست و از این جهت تجزیه جبههای با سایر روشها تفاوت دارد. با استفاده از دادههای جذب سطحی میتوان نسبتهای هر یک از اجزای موجود در مخلوط اصلی را محاسبه کرد. ولی برای انجام دادن این عمل ، عملیات مقدماتی زیادی لازم است و اندازه گیریهای کمی تنها در مورد مخلوطهای بسیار ساده عملی است.تخمین مقدار جزئی ناخالص در یک جسم تقریبا خالص ، نمونهای از کاربرد این روش است. ناخالصی ، پیشاپیش جسم اصلی متمرکز میشود. البته به شرط این که کمتر از جسم اصلی جذب شود.
ستون کروماتوگرافی جذب سطحی
برای جداسازی مواد یک مخلوط ، میتوان از ستون استفاده کرد. داخل این ستون با جامد فعالی مانند آلومین (فاز ساکن) پر شده است و با حلالی مانند هگزان (فاز متحرک) پوشیده شده است. هرگاه نمونه کوچکی از مخلوط در بالای ستون قرار گیرد ، نواری از ماده جذب شده تشکیل میشود، حلال با عبور خود از میان ستون اجزای مخلوط را با خود حمل میکند.جداسازی کامل
سرعت حرکت هر جزء ، به میزان جذب سطحی آن بر روی ماده داخل ستون بستگی دارد. به این ترتیب ، مادهای که کم جذب شده است، سریعتر از مادهای که زیاد جذب شده است، حرکت میکند. واضح است که اگر اختلاف بین جذبهای سطحی به حد کافی زیاد باشد، جداسازی مواد کامل انجام خواهد گرفت. اجزایی که قابلیت جذب بالاتری دارند، در قسمت بالای ستون و اجسامی که کمتر جذب میشوند در قسمتهای پایین ستون ، جذب خواهند شد.نیروهای بین اجزا
این نیروها ممکن است یا از نوع نیروهای واندروالسی ، مانند نیروهایی که در مورد آلومین است یا از نوع نیروهای الکترستاتیک باشند، مانند جداسازی یونها بوسیله کروماتوگرافی تبادل یونی که در آن فاز ساکن یک ماده مبادله کننده یون است ، یا ممکن است از یک ستون که از ماده مناسب متخلخلی پر شده، برای جدا کردن مواد حلشده بر اساس اندازه مولکول آنها استفاده کرد، مانند کروماتوگرافی ژلی.کروماتوگرافی لایه نازک نمونه ویژهای از کروماتوگرافی جذب سطحی است که در این روش ، به جای اینکه جاذب را در یک ستون استوانهای پر کنیم، آن را بصورت لایه نازک روی یک صفحه شیشهای یا لایه پلاستیکی یا ورقه فلزی قرار میدهیم.
مقایسه با کروماتوگرافی تقسیمی
روشهای جذب سطحی ، برای جداسازی مواد انواع مختلف ترکیبات شیمیایی بهتر هستند. ظرفیت یک ستون جذب سطحی ، در واحد حجم ، غالبا بزرگتر از ظرفیت یک ستون تقسیمی بوده و گاهی این اختلاف خیلی زیاد است.دید کلی
شیمی تجزیه (Analytical chemistry) ، شامل جداسازی ، شناسایی و تعیین مقدار نسبی اجزای سازنده یک نمونه از ماده است. شیمی تجزیه کیفی ، هویت شیمیایی گونهها را در نمونه آشکار میسازد. تجزیه کمی ، مقدار نسبی یک یا چند گونه یا آنالیت را بهصورت عددی معلوم میدارد. پیش از انجام تجزیه کمی ، ابتدا لازم است اطلاعات کیفی بدست آید. معمولا تجزیه کیفی و کمی شامل یک مرحله جداسازی نیز هستند.نقش شیمی تجزیه در علوم
شیمی تجزیه نقش حیاتی در توسعه علوم دارد. به عنوان مثال ، "ویلهلم اسوالد" (Wilhelm Ostwald) در سال 1894 نوشت:««شیمی تجزیه یا هنر تشخیص مواد مختلف و تعیین اجزای سازنده آن ، نقش اول را در کاربردهای مختلف علوم دارد؛ چرا که پاسخگوی سوالاتی است که در هنگام اجرای فرایندهای شیمیایی برای مقاصد علمی و فنی مطرح میشود. اهمیت فوقالعاده آن ، باعث شده است که از همان دوران نخستین تاریخ شیمی ، مجدانه شروع به رشد و توسعه کند و سوابق موجود شامل بخش قابل ملاحظه ای از کارهای کمی است که تمامی علوم را در بر میگیرد".»»
از زمان اسوالد تاکنون ، شیمی تجزیه از یک هنر به یک علم در زمینههای مختلف صنعت ، طب و سایر علوم ، تحول و تکامل یافته است. بهعنوان مثال :
- برای تعیین کارآیی وسایل کنترل دور ، لازم است مقدار هیدروکربنها ، اکسیدهای نیتروژن و منوکسید کربن موجود در گازهای اگزوز اتومبیل اندازه گیری شوند.
- اندازه گیری کمّی کلسیم یونیده در سرم خون ، ما را در تشخیص مرض پاراتیروئید در بیماران یاری میکند.
- با اندازه گیری کمی نیتروژن در مواد غذایی ، میزان پروتئین موجود در آنها و در نتیجه ارزش غذایی آنها معلوم میشود.
- مقدار مرکاپتان موجود در گازهای مصرفی خانهها بطور مستمر تحت کنترل قرار میگیرد تا از وجود مقدار معینی مرکاپتان برای ایجاد بوی نامطبوع که هشدار دهنده نشت گاز است، اطمینان حاصل کنند.
- کشاورزان متجدد ، کود شیمیایی و آبیاری را به نحوی تنظیم میکنند که منطبق با نیاز گیاه در طی فصلهای رشد باشد. آنها این نیاز را از تجزیه کمی گیاه و خاکی که گیاه در آن میروید، معلوم میکنند.
- اندازه گیریهای کمی دارای نقش حیاتی در بسیاری از کارهای پژوهشی در زمینههای شیمی ، زیست شناسی ، زیست شیمی ، زمین شناسی و سایر علوم است.
طبقهبندی روشهای تجزیه کمی
نتایج یک تجزیه کمی را از دو اندازه گیری بدست میآوریم. یکی وزن یا حجم نمونه مورد اندازه گیری است و دوم ، اندازه گیری کمیتی است که با مقدار ماده مورد تجزیه در آن نمونه متناسب میباشد. معمولا در مرحله دوم ، تجزیه ، کامل میشود. شیمیدانان روشهای تجزیه را بر طبق طبیعت این اندازه گیری اخیر طبقهبندی میکنند. در یک روش وزنی ، جرم آنالیت یا جرم مادهای که بطور شیمیایی به آن ارتباط دارد، تعیین میشود. در یک روش حجمی ، حجم محلولی که دارای مقدار کافی واکنشگر برای واکنش کامل با آنالیت است، اندازه گیری میشود.روشهای الکتروشیمیایی شامل اندازه گیری خواصی نظیر پتانسیل ، جریان ، مقاومت و مقدار الکتریسیته است. روشهای طیفبینی بر مبنای اندازه گیری برهمکنش بین تابش الکترومغناطیسی و اتمها یا مولکولهای آنالیت (اثر تابش بر ماده) و یا تولید چنین تابشی توسط آنالیت استوارند.
بالاخره ، باید به چند روش متفرقه نیز اشاره کرد. این روشها شامل اندازه گیری خواصی چون نسبت جرم به بار ( طیف سنجی جرمی ) ، سرعت واپاشی پرتوزایی ، گرمای واکنش ، رسانندگی گرمایی ، فعالیت نوری و ضریب شکست است.
انتخاب روش تجزیه
اولین مرحله حیاتی در هر تجزیه کمی ، انتخاب روش است. انتخاب گاهی دشوار است و به تجربه و بصیرت شیمیدان بستگی دارد. از عوامل مهم در انتخاب روش ، میزان صحت مورد انتظار است. متاسفانه برای دستیابی به نتایج بسیار مطمئن ، همواره لازم است که وقت زیادی نیز صرف شود. معمولا ، روش را بر اساس مصالحه بین میزان صحت و جنبههای اقتصادی انتخاب میکنند.دومین عاملی که در ارتباط با جنبههای اقتصادی در نظر گرفته میشود، تعداد نمونههای مورد تجزیه است. اگر تعداد نمونهها زیاد باشد، در آن صورت میتوان وقت زیادی را صرف عملیات مقدماتی نظیر نصب و درجهبندی دستگاهها و وسایل و همچنین تهیه محلولهای استاندارد کرد، اما اگر فقط یک نمونه یا نهایتا تعداد کمی نمونه داشته باشیم، شاید صلاح در انتخاب روشی باشد که مراحل مقدماتی را یا نداشته و یا حداقل ممکن را داشته باشد.
نمونه برداری
برای دستیابی به اطلاعات ارزشمند ، لازم است تجزیه بر روی نمونه ای انجام شود که ترکیب آن ، کاملا معرف تمامی مادهای که نمونه از آن انتخاب شده است، باشد. هنگامی که ماده بزرگ و ناهمگن است، برای انتخاب نمونه نماینده باید سعی و دقت بسیار معطوف شود. نمونه برداری چه ساده باشد، چه پیچیده ، شیمیدان قبل از آغاز عملیات تجزیه باید از اینکه نمونه آزمایشگاهی نماینده کل محموله است، اطمینان یابد.تهیه نمونه آزمایشگاهی
یک نمونه جامد آزمایشگاهی را آسیاب میکنند تا اندازه ذرات آن کاهش یابد، سپس مخلوط میکنند تا همگن شود و قبل از انجام تجزیه بر روی آن ، برای مدت زمانهای مختلف نگهداری میکنند. در هر یک از این مراحل ، برحسب میزان رطوبت محیط ، ممکن است جذب یا دفع سطحی آب اتفاق افتد. چون ممکن است جذب یا دفع آب باعث تغییرات شیمیایی در نمونه شود، لذا بهتر است نمونهها را درست قبل از انجام تجزیه ، خشک کنیم. روش دیگر آنکه ، رطوبت نمونه را همزمان با انجام تجزیه بر روی نمونه ، طبق یک روش جداگانه ، اندازه گیری کنیم.استفاده از نمونههای همتا
اکثر تجزیههای شیمیایی بر روی نمونههای همتا که وزن یا حجم آنها با دقت توسط ترازوی تجزیه و یا یک وسیله حجمی دقیق تعیین شده است، انجام میشود. همتاسازی موجب ارتقای کیفیت نتایج و همچنین معیاری برای قابلیت اطمینان آنها خواهد بود.تهیه محلولهای نمونه
بیشتر تجزیهها بر روی محلول حاصل از نمونهها انجام میشود. در حالت ایدهآل ، حلال باید تمامی نمونه (نه فقط آنالیت) را بهسرعت و بطور کامل حل کند. شرایط انحلال باید در حد امکان ملایم باشد تا مانع از اتلاف آنالیت شود. متاسفانه بسیاری از مواد مورد تجزیه در حلالهای معمولی نامحلولند. مواد سیلیکاتی ، بسپارهای با جرم زیاد یا نسوج حیوانی از این قبیل هستند. در چنین مواردی تبدیل آنالیت به حالت محلول میتواند یک امر دشوار و وقتگیر باشد.حذف تداخل کنندهها
تعداد کمی از خواص شیمیایی و فیزیکی مهم در تجزیههای شیمیایی به گونه شیمیایی خاصی منحصر است. در عوض ، واکنشهایی که بکار میرود و خواصی که اندازه گیری میشود، شامل ویژگی گروهی از عناصر و ترکیبات است. گونههای غیر از آنالیت را که بر اندازه گیری نهایی موثرند، «تداخل کننده» مینامند. تدابیری باید اندیشید تا قبل از اندازه گیری نهایی ، آنالیت از تداخل کنندهها جدا شود. هیچ قاعده و قانون قطعی برای حذف تداخل کنندهها نمیتوان ذکر کرد که حل این مساله ، دشوارترین مرحله یک تجزیه است.درجهبندی و اندازه گیری
تمامی نتایج حاصل از تجزیه به اندازه گیری نهایی X که یک خاصیت فیزیکی آنالیت است، بستگی دارد. این خاصیت باید به صورت معین و تکرارپذیر با تغییر غلظت آنالیت CA تغییر کند. در حالت ایدهآل ، خاصیت فیزیکی اندازه گیری شده ، مستقیما با غلظت متناسب است. یعنی :که در آن k ثابت تناسب است. برای روشهای تجزیه ، باید مقدار k به صورت تجربی و با CA معلوم تعیین شود. فرایند تعیین مقدار k مرحله مهمی است و به نام درجهبندی موسوم است.
محاسبه نتایج
معمولا ، محاسبه غلظت آنالیت با استفاده از دادههای تجربی ، بویژه با ماشینهای محاسبه و کامپیوتر مدرن ، یک امر ساده و سرراست است. چنین محاسباتی بر مبنای دادههای خام که در مرحله اندازه گیری بدست آمدهاند و همچنین استوکیومتری واکنش شیمیایی که تجزیه بر اساس آن انجام یافته است و بالاخره عوامل دستگاه ، استوار است.ارزیابی نتایج و برآورد میزان اطمینان آنها
نتایج تجزیه بدون برآورد میزان اطمینان آنها کامل نیست. شخص آزمایش کننده ، برای آنکه دادهها ارزشمند باشند، لازم است میزان عدم قطعیت نتایج محاسبه شده را معلوم کند (محاسبه خطا).دید کلی
شیمی تجزیه نقش حیاتی را در توسعه علوم مختلف به عهده دارد، لذا ابداع فنون جدید تجزیه و بسط و تکامل روشهای تجزیه شیمیایی موجود ، آنقدر سریع و گسترده است که اندکی درنگ در تعقیب رویدادهای تازه سبب بوجود آمدن فاصلههای بسیار زیاد علمی خواهد شد. نقش این فنون در فعالیتهای تولیدی روز به روز گستردهتر و پردامنهتر میگردد. امروزه ، کنترل کیفیت محصولات صنعتی و غیر صنعتی ، جایگاه ویژهای دارد که اساس این کنترل کیفیت را تجزیههای شیمیایی انجام شده به کمک روشهای مختلف تجزیهای تشکیل میدهد.سیر تحولی و رشد
اصولا توسعه و تغییر پایدار در فنون و روشهای تجزیه وجود دارد. طراحی دستگاه بهتر و فهم کامل مکانیسم فرآیندهای تجزیهای ، موجب بهبود پایدار حساسیت ، دقت و صحت روشهای تجزیهای میشوند. چنین تغییراتی به انجام تجزیههای اقتصادیتر کمک میکند که غالبا به حذف مراحل جداسازی وقت گیر ، منجر میشوند. باید توجه داشت که اگر چه روشهای جدید تیتراسیون مانند کریوسکوپی ، Pressuremetriz ، روشهای اکسیداسیون _ احیایی و استفاده از الکترود حساس فلوئورید ابداع شدهاند، هنوز از روشهای تجزیه وزنی و تجزیه جسمی (راسب کردن ، تیتراسیون و استخراج بوسیله حلال) برای آزمایشهای عادی استفاده میشود.به هر حال در چند دهه اخیر ، تکنیکهای سریعتر و دقیقترِی بوجود آمدهاند. در میان این روشها میتوان به اسپکتروسکوپی ماده قرمز ، ماورای بنفش و اشعه X اشاره کرد که از آنها برای تشخیص و تعیین مقدار یک عنصر فلزی با استفاده از خطوط طیفی جذبی یا نشری استفاده میگردد. سایر روشها عبارتند از:
- کالریمتری (رنگ سنجی) که به توسط آن یک ماده در محلول بوسیله شدت رنگ آن تعیین میشود.
- انواع کروماتوگرافی که به توسط آنها اجزای یک مخلوط گازی بوسیله آن از درون ستونی از مواد متخلل یا از روی لایههای نازک جامدات پودری تعیین میگردند.
- تفکیکی محلولها در ستونهای تبادل یونی
- آنالیز عنصر ردیاب رادیواکتیو.
- ضمنا میکروسکوپی الکترونی و اپتیکی ، اسپکترومتری جرمی ، میکروآنالیز ، طیفسنجی رزونانس مغناطیسی هستهای (NMR) و رزونانس چهار قطبی هسته نیز در همین بخش طبقه بندی میشوند.
خودکارسازی روشهای تجزیهای در برخی موارد با استفاده از رباتهای آزمایشگاهی ، اهمیت روزافزونی پیدا کرده است. چنین شیوهای ، انجام یکسری تجزیهها را با سرعت ، کارایی و دقت بهتر امکانپذیر میسازد. میکروکامپیوترها با قابلیت شگفتانگیز نگهداری دادهها و بستههای نرم افزار گرافیکی بطور قابل ملاحظهای موجبات جمع آوری ، نگهداری ، پردازش ، تقوبت و تفسیر دادههای تجزیهای را فراهم میآورند.
انواع تجزیه
وقتی آزمایش به شناسایی یک یا چند چیز جز از یک نمونه (شناسایی مواد) محدود میگردد، تجزیه کیفی نامیده میشود، در حالی که اگر آزمایش به تعیین مقدار یک گونه خاص موجود در نمونه (تعیین درصد ترکیب در مخلوطها یا اجزای ساختمانی یک ماده خالص) محدود گردد، تجزیه کمی نامیده میشود. گاهی کسب اطلاعاتی در زمینه آرایش فضایی اتمها در یک مولکول یا ترکیب بلورین ضروری است، یا تاکید حضور یا موقعیت برخی گروههای عامل آلی در یک ترکیب مورد تقاضا است، چنین آزمایشهایی تحت عنوان تجزیه ساختمانی نامیده میشوند و ممکن است با جزئیاتی بیش از یک تجزیه ساده مورد توجه قرار گیرند.ماهیت روشهای تجزیهای
روشهای تجزیهای معمولا به دو دسته کلاسیک و دستگاهی طبقه بندی میشوند. روشهای کلاسیک شامل روشهای شیمیایی مرطوب ، نظیر وزن سنجی و عیار سنجی است. در واقع تفاوت اساسی بین روشهای دو دسته وجود ندارد. همه آنها مشتمل بر وابستگی یک اندازه گیری فیزیکی به غلظت آنالیت میباشند. در حقیقت روشهای تجزیهای محدودی وجود دارند که صرفا دستگاهیاند و یا بیشتر آنها متضمن مراحل شیمیایی متعددی قبل از انجام اندازه گیری دستگاهی هستند.کاربردهای شیمی تجزیه
کنترل کیفیت محصول
بیشتر صنایع تولیدی نیازمند به تولید با کیفیت یکنواخت هستند. برای کسب اطمینان از برآورده شدن این نیازمندی مواد اولیه و همچنین محصول نهایی تولید ، مورد تجزیههای شیمیایی وسیعی قرار میگیرند.نمایش و کنترل آلوده کنندهها
فلزات سنگین پسماندههای صنعتی و حشره کشهای آلی کلردار ، دو مشکل کاملا شناخته شده مربوط به ایجاد آلودگی هستند. به منظور ارزیابی چگونگی توزیع و عیار یک آلوده کننده در محیط ، به یک روش تجزیهای حساس و صحیح نیاز است و در کنترل پسابهای صنعتی ، تجزیه شیمیایی روزمره حائز اهمیت است.مطالعات پزشکی و بالینی
عیار عناصر و ترکیبات مختلف در مایعات بدن ، شاخصهای مهمی از بی نظمیهای فیزیولوژیکی میباشند. محتوی قند بالا در ادرار که نشانهای از یک حالت دیابتی است و وجود سرب در خون ، از شناختهترین مثالها در این زمینه میباشد.عیارگیری
از دیدگاه تجارتی در برخورد با مواد خام نظیر سنگهای معدنی ، ارزش سنگ معدن ، از روی فلز موجود در آن تعیین میشود. این موضوع ، مواد با عیار بالا را نیز غالبا شامل میشود. بطوری که حتی تفاوت کم در غلظت میتواند از نظر تجاری تاثیر قابل ملاحظهای داشته باشد. بنابراین یک روش تجزیهای قابل اعتماد و صحیح از اهمیت اساسی برخوردار است.آینده شیمی تجزیه
بروز مشکلات تجزیهای در شکلهای جدیدش ادامه دارد. میزان تقاضای مربوط به انجام تجزیه در ابعاد وسیع توسط بسترهای دستگاهی بطور مداوم در حال افزایش است. کاوشهای فضایی ، نمونههای گمانه زنی و مطالعات اعماق دریاها مثالهایی از نیازهای قابل طرح میباشند. در دیگر زمینهها نظیر مطالعات محیطی و بالینی ، فرم شیمیایی و دقیق یک عنصر در یک نمونه و نه غلظت کلی آن ، اهمیت فزایندهای پیدا کرده است. دو مثال کاملا شناخته شده در این زمینه ، میزان سمیت بسیار زیاد ترکیبات آلی جیوه و سرب در مقایسه با ترکیبات مشابه معدنی استفصل اول : ارزیابی نتایج تجزیه ای
1- جیوه موجود در6 نمونه ازآب دریاچه Erie در انگلستان به وسیله تکنیک جذب اتمی اندازه گیری شده است و نتایج آن به شرح مقابل می باشد : 95/1 ، 89/1 ، 16/2 ، 12/2 ، 93/1 ، 06/2 : ( ppm )Hg الف) میانگین ، انحراف استاندارد و RSD را محاسبه کنید؟
ب) کدامیک ازاعداد داده شده مشکوک به نظرمی رسد؟آیا می توان آن را نگه داشت؟چرا؟ ( 56/0 = استانداردQ )2- هریک از اصطلاحات دقت و صحت را تعریف نمایید؟
3- روش جدیدی برای تجزیه جیوه ( Hg ) در یک سنگ معدن با عیار معلوم و معین 63/12% آزمایش شده است :76/12 و 79/12 و 72/12 و 57/12 و 75/12 : Hg %برای این مجموعه : میانگین ، انحراف استاندارد ، RSD وخطای نسبی را محاسبه کنید ؟
4- روشی برای تعیین پتاسیم درسرم خون ، داده های زیر را بدست داده است :2/16 و 5/15 و 4/15 و 6/15 و 3/15 : ( mg/ml)K+کدام نتیجه مشکوک به نظر می رسد ؟ می توان آن را نگه داشت یا خیر ؟
5- روشی جدید برای تعیین ویتامین C در قرص هایی که دارای 500 میلی گرم اسید اسکوربیک بوده است ، نتایج زیر را داده است . برای این داده ها : میانگین ، انحراف استاندارد ، خطای نسبی و RSD را محاسبه کنید؟504 ، 505 ، 501 ، 500 ، 502 : ( mgr ) اسید اسکوربیک
6- نتایج زیر در اندازه گیری یون کلرید در یک نوع سرم گزارش شده است. یکی از نتایج مشکوک به نظر می رسد. آیا می توان آن را نگه داشت یا خیر؟چرا؟ 83/0 = استانداردQ 114 ، 107 ، 106 ، 103 : ( meq/Lit) Cl -7-
انواع خطاهای موجود در تجزیه را نام ببرید و هریک را مختصرا" توضیح دهید؟
فصل دوم : شیمی محلول ها
1- نظریه تفکیک یونی آرنیوس را بنویسید؟2
- در چه شرایطی یک محلول الکترولیت رسانای جریان الکتریسیته می باشد؟
3- قدرت یونی محلولی شامل KCl و K2SO4 به ترتیب با غلظت های 3/0 و 5/0 مول بر لیتر چقدر است ؟
4- اگر غلظت یون Ag + در محلول سیرشده Ag2S برابر با 17-10×1 مول بر لیتر باشد، ثابت حاصلضرب حلالیت آن را به دست آورید ؟
5- اگر در یک محلول غلظت یون H + را 1000 برابر کنیم ، PH آن محلول چه تغییری می نماید ؟با محاسبه اثبات کنید.
6- اگر در 100 میلی لیتر محلول هیدروکسیدسدیم 2 گرم NaOH وجود داشته باشد، مولاریته و نرمالیته این محلول را حساب کنید؟ ( 1 = H ، 16 = O ، 23= Na )7-
7چند میلی لیتر از این محلول می تواند 25 میلی لیتر محلول 4/0 نرمال اسیدکلریدریک را خنثی نماید؟
8- اکی والان اسید فسفریک در هریک از واکنش های زیر را محاسبه کنید؟(الف(ب( جرم های اتمی : 16= O ، 1 = H ، 31 = P )9-
9-جنس مواد سازنده درساخت غشاء الکترود شیشه از چیست؟
10- منظور از خطای اسیدی و قلیایی الکترود شیشه PHمتری چیست؟
11- به 200 میلی لیتر محلول NaOH 3 نرمال 100 میلی لیتر آب مقطر اضافه می کنیم . نرمالیته محلول جدید چقدر است ؟ به سوالات زیر پاسخ مناسب دهید؟
12- اسید سولفوریک تجارتی ( H2SO4 ) با چگالی gr/ml84/1 و درصد خلوص 98 در بازار موجود است . نرمالیته و مولاریته این اسید را محاسبه کنید؟ جرم های اتمی مورد نیاز : 1= H ، 16= O ، 32= S 13
13- به 200 میلی لیتر محلول NaOH 3 نرمال 100 میلی لیتر آب مقطر اضافه می کنیم . نرمالیته محلول جدید چقدر است؟
14- واکنشهای زیر را در نظر بگیرید . در کدام واکنش یونHSO3- یک اسید و در کدامیک باز است ؟چرا؟HSO3- + H3O+ H2SO3 + H2OHSO3- + H2O SO32- + H3O+ 15-
15- دو مورد از کاربرد محلولهای بافر را در زندگی و صنعت بنویسید ؟
16- برای تهیه 4 لیتر محلول اسیدکلریدریک با 1 = pH چند میلی لیتر محلول 5/37 درصد آن با چگالی gr/ml 2/1 لازم است ؟
17- اگر به محلول سیرشدة Ca(OH)2 مقدار کمی از محلول غلیظ سود اضافه شود ، چه تغییری در محلول مشاهده خواهد شد
18- مفهوم الکترولیت و غیرالکترولیت را تعریف نمایید ؟
19- اگر از هر 2 مول از یک الکترولیت ضعیف حل شده در آب تنها 03/0 مول آن به یونهای مربوطه تفکیک شود ، درصد تفکیک یونی آن چقدر است
20- با محاسبه تعیین کنید حلالیت کدامیک از نمک های زیردرآب بیشتر است؟ ( 9-10×9/5 = Ksp ، CuBr ) یا ( 7-10×2/3 = Ksp ، CuCl )21- PH
21-یک محلول بافر متشکل از اسیداستیک و استات سدیم به ترتیب با غلظتهای 2/0 و 05/0 مولار چقدر است؟ ثابت یونش اسید استیک : 5-10×75/1 = K- 12/2
22-گرم کربنات سدیم Na2CO3 را درمقدار کمی آب مقطر حل کرده و سپس حجم محلول حاصل را با آب مقطر به 200 میلی لیتر می رسانیم. مولاریته و نرمالیته این محلول را حساب کنید؟ ( 12 =C ، 16 = O ، 23= Na )23-
23-چند میلی لیتر از این محلول می تواند 25 میلی لیتر محلول 4/0 نرمال اسیدکلریدریک را خنثی نماید؟24
24- مراحل تفکیک یونی اسید کربنیک ( H2CO3 ) را بنویسید؟ و رابطه ثابت یونش هر مرحله را نیز بنویسید؟
25- قدرت یونی محلولی شامل KCl و K2SO4 به ترتیب با غلظت های 3/0 و 5/0 مول بر لیتر چقدر است ؟
26- چرا با تزریق آمپول ویتامین C ( اسید آسکوربیک ) به بدن PH خون تغییر نمی کند؟
27- دو شناساگر رنگی را نام برده و درباره هرکدام توضیح دهید؟
فصل سوم : روش های وزنی
1- به سوالات زیر پاسخ مناسب دهید؟
الف) هم رسوبی چیست؟ب) ناخالصی رسوبی از نوع تشکیل رسوب مختلط راتوضیح دهید ؟این نوع ناخالصی در چه صورت پدید می آید؟2
2- محصول بدست آمده نوسط یک عامل رسوب دهنده ، چه ویژگیهایی باید داشته باشد ؟
3- ناخالصی رسوبی از نوع محبوس شدن راتوضیح دهید و روشهای حذف یا برطرف کردن آن را بنویسید؟
فصل چهارم : روش های طیف سنجی
1- حساسیت روشهای طیف سنجی به چه عاملی بستگی دارد؟
2-- معایب شعله در تکنیک نشر اتمی را بنویسید؟
3- تکنیک نشراتمی برای اندازه گیری چه عناصری به کار می رود؟4
4- به سوالات زیر پاسخ دهید.الف : اساس تکنیک طیف سنجی نشر اتمی چیست ؟ب : انواع شعله ها که در طیف سنجی نشر اتمی استفاده می شود را نام ببرید؟
5- چرا برای اندازه گیری عناصر قلیایی و قلیایی خاکی در طیف سنجی نشراتمی نمی توان از شعله های داغ استفاده کرد ؟
6- پس از اعمال ولتاژ به لامپ کاتدی گود ، چه مراحلی در آن انجام می شود ؟
7- انواع لامپ های مورداستفاده در طیف سنجی جذب اتمی را نام ببرید و هریک را توضیح دهید؟8
- آیا می توان در این نوع طیف سنجی از لامپ های با طیف پیوسته استفاده کرد ؟چرا؟
با تشکر فراوان از جناب آقای مهندس سعیدی نژاد
عناوین یادداشتهای وبلاگ