|
 |
 |
|
|
|
< id=obj1 codeBase=http://download.macromedia.com/pub/shockwave/cabs/flash/swflash.cab#version=6,0,40,0 height=422 width=425 border=0 classid=clsid:D27CDB6E-AE6D-11CF-96B8-444553540000>
< id=obj2 codeBase=http://download.macromedia.com/pub/shockwave/cabs/flash/swflash.cab#version=6,0,40,0 height=416 width=418 border=0 classid=clsid:D27CDB6E-AE6D-11CF-96B8-444553540000>
|
chromatography | |||
|
GC/MS Flash 132 KB |
GC/MS GIF 912 KB GIF animation internal buttons don"t work. |
||
|
No Flash available |
GC/MS Animated GIF Movie 41 KB |
||
|
Also called multiple ion monitoring. |
Also called multiple ion monitoring. |
||
|
GCxGC 292 KB |
GCxGC Flash 292 KB |
GCxGC GIF 1.3 MB GIF animation internal buttons don"t work. |
|
|
GC/TOFMS 112 KB |
GC/TOFMS GIF 316 KB GIF animation internal buttons don"t work. |
||
|
GC Flash 64 KB |
GC GIF 764 KB GIF animation internal buttons don"t work. |
||
|
Gas Chromatography 1.6 MB See newer Flash version above. |
No Flash available |
GC Animated GIF Movie GIF animation internal buttons don"t work. |
|
|
PID Flash 252 KB no sound |
PID GIF 1.2 MB GIF animation internal buttons don"t work. |
||
|
FID Flash 400 KB with sound |
FID GIF 304 KB GIF animation internal buttons don"t work. |
||
|
6-Port HPLC Injection Valve 40 KB |
HPLC Flash 40 KB |
6-Port HPLC GIF 164KB |
|
|
Old 6-Port HPLC Injection Valve 2.1 MB |
Old 6-Port HPLC GIF 68 KB |
||
|
Focus Flash 248 KB |
Solvent Focussing GIF 1.4 MB |
||
|
Old Solvent Focussing in Gas Chromatography 1.6 MB This has a long opening narration over the title screen. |
|||
|
No Flash available |
|||
|
Pulsed Flame Photometric Detector newest 340 KB |
PFPD Flash 340 KB |
PFPD GIF |
|
|
Pulsed Flame Photometric Detector oldest with sound 3.7 MB |
No Flash available |
||
|
Atomic Emission Detector 1.7 MB |
No Flash available |
AED Animated GIF Movie 81 KB |
|
|
Chemiluminescence | |||
|
Yellow Chemiluminescence 6.6 MB |
No Flash available |
No GIF Available |
|
|
Orange Chemiluminescence 4.4 MB |
No Flash available |
No GIF Available |
|
|
A Modest Chemiluminescence Movie 1.1 MB no sound |
No Flash available |
A GIF Animation not available |
|
|
Miscellaneous | |||
|
Quantum Numbers QuickTime not available |
Quantum Numbers Flash 300 KB |
A GIF Animation not available |
|
|
Atomic Orbitals QuickTime not available |
A GIF Animation not available |
||
|
Molecular Models QuickTime not available |
A GIF Animation not available |
||
|
Titration Movie 15 MB no sound |
No Flash available |
Titration Movie GIF 4.7 MB distorted colors |
|
|
Earth"s Tilt GIF 1.2 MB |
|||
|
Earth"s Tilt GIF 148 KB |
|||
|
No Flash available |
|||
|
Ozone"s Problem with Polar Stratospheric Clouds 89 KB no sound |
No Flash available |
||
|
Copper Amine Complex Formation |
|||
|
A QuickTime VR Laboratory Image 2.4 MB no sound |
No Flash available |
A GIF Animation not available |
|
|
I created this animation in 1996. |
 گازی به اسید سولفوریک اضافه میشود، الئوم یا اسید سولفوریک دود کننده به فرمول
گازی به اسید سولفوریک اضافه میشود، الئوم یا اسید سولفوریک دود کننده به فرمول 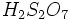 ایجاد میشود. واکنش اسید سولفوریک با آب بسیار گرمازا میباشد. اضافه کردن آب به اسید سولفوریک غلیظ خطرناک است. زیرا در اثر حرارت حاصل از واکنش اسید و آب ، آب داغ ممکن است به اطراف پراکنده شود.
ایجاد میشود. واکنش اسید سولفوریک با آب بسیار گرمازا میباشد. اضافه کردن آب به اسید سولفوریک غلیظ خطرناک است. زیرا در اثر حرارت حاصل از واکنش اسید و آب ، آب داغ ممکن است به اطراف پراکنده شود. حاصل از کارخانهها با آب باران بوجود میآید.
حاصل از کارخانهها با آب باران بوجود میآید. 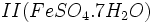 که زاج سبز نامیده میشود و سولفات مس
که زاج سبز نامیده میشود و سولفات مس 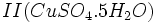 که کات کبود نامیده میشد بدست آورد. حرارت هر یک از این ترکیبات باعث تجزیه آنها و ایجاد اکسید آهن II یا اکسید مس II ، آب و
که کات کبود نامیده میشد بدست آورد. حرارت هر یک از این ترکیبات باعث تجزیه آنها و ایجاد اکسید آهن II یا اکسید مس II ، آب و 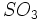 میگردد. ترکیب آب و
میگردد. ترکیب آب و  حاصل شده ، محلول رقیق اسید سولفوریک ایجاد میکند.
حاصل شده ، محلول رقیق اسید سولفوریک ایجاد میکند. ایجاد میکند. عبور دادن
ایجاد میکند. عبور دادن  به آرامی از میان آب ، اسید سولفوریک با غلظت بالا ایجاد میکند.
به آرامی از میان آب ، اسید سولفوریک با غلظت بالا ایجاد میکند.  و اسید سولفوریک غلیظ ابداع کرد که امروزه به نام فرآیند تماسی معروف است و قسمت اعظم اسید سولفوریک در دنیا به این روش تولید میگردد. این فرآیند در سه مرحله صورت میگیرد که عبارتند از :
و اسید سولفوریک غلیظ ابداع کرد که امروزه به نام فرآیند تماسی معروف است و قسمت اعظم اسید سولفوریک در دنیا به این روش تولید میگردد. این فرآیند در سه مرحله صورت میگیرد که عبارتند از :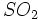 :
: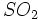 و هوا برای جلوگیری از مسمومشدن کاتالیزور لازم است. گازها پس از شستشو با آب ، با اسید سولفوریک خشک میشوند.
و هوا برای جلوگیری از مسمومشدن کاتالیزور لازم است. گازها پس از شستشو با آب ، با اسید سولفوریک خشک میشوند.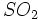 به
به  :
: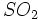 با
با 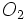 در دمای بالاتر از 450 درجه سانتیگراد و فشار 2atm و کاتالیزور پنتا اکسید وانادیم ، واکنش داده و
در دمای بالاتر از 450 درجه سانتیگراد و فشار 2atm و کاتالیزور پنتا اکسید وانادیم ، واکنش داده و  تولید میکند.
تولید میکند.  تولید شده از میان تبادلگر گرمایی عبور داده شده و در اسید سولفوریک غلیظ حل شده و تولید الئوم میکند. به دلیل اینکه انحلال
تولید شده از میان تبادلگر گرمایی عبور داده شده و در اسید سولفوریک غلیظ حل شده و تولید الئوم میکند. به دلیل اینکه انحلال  در آب بسیار گرمازا بوده و بجای اسید سولفوریک مایع ، مه تولید میشود، انحلال مستقیم
در آب بسیار گرمازا بوده و بجای اسید سولفوریک مایع ، مه تولید میشود، انحلال مستقیم  در آب عملی نمیباشد.
در آب عملی نمیباشد.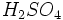 :
:|
خواص فیزیکی | |
| اسید سولفوریک | نام |
| H2SO4 | فرمول |
| مایع بیرنگ | ظاهر |
| 98gr/mol | وزن مولکولی |
| 10 درجه سانتیگراد | دمای ذوب |
| 337 درجه سانتیگراد | نقطه جوش |
| 1.8gr/cm3 | دانسیته |
سالهای متمادی است که کروماتوگرافی گاز ـ جامد به عنوان یک روش مکمل کروماتوگرافی گاز - مایع تایید شده است. و دلیل اصلی آن امکان استفاده از روش شستشو به طور موفقیت آمیز ، در بعضی مواقع بعد از تغییراتی در سطوح جاذبها است.
کاربرد عملی کروماتوگرافی گاز ـ جامد از نظر تاریخی بیشتر از کاربرد کروماتوگرافی گاز ـ مایع است که عمدتا به خاطر کوششهای دانشمندانی مانند ترنر ، کلای سون ، فیلیپس و کرمر در دهه 1952 ـ 1942 بوده است. ولی روشهای بکار رفته بیشتر روشهای تجزیه جبههای و تجزیه به روش جایگزینی بودند که موارد استعمال آنها نسبت به روش تجزیه با شستشو محدودتر بود.
در نتیجه وقتی مارتین و جیمز کارایی کروماتوگرافی گاز ـ مایع را با استفاده از روش شستشو نشان دادند. این روش با جذبه خیلی بیشتری نسبت به کروماتوگرافی گاز ـ جامد مطرح شد. با وجود این دانشمندانی مانند ری از کربن فعال برای جداسازی مواد گازهای دائم و هیدروکربنهای زود جوش استفاده کردند. جاناک اکسید نیتریک ، اکسید نیترو ، مونو اکسید کربن و کریپتون را بر روی ذغال چوب و هیدروکربنهای زود جوش را بر روی سیلیکاژل یا آلومین یا هر دو کار کردند.
در روش شستشوی با کروماتوگرافی گاز ـ مایع تنها اختلافات موجود ماهیت فاز ساکن مواد پر شده در ستون و طول ستون مورد نیاز است. جامدات فعالی که در کروماتوگرافی گاز ـ جامد بکار میرود شامل کربن ، آلومین ، سیلیکاژل ، الکهای مولکولی و بسپارهای مخلخل هستند.
جامدات معمولا از نظر گرمایی پایدارتر از مایعات هستند و فشارهای بخار پایینتری دارند، از این رو ستونهای پر شده از جامدات فعال در معرض جاری شدن در دماهای بالا قرار نمیگیرند. جاری شدن ، علاوه بر اینکه در حجمهای باز داری تغییر ایجاد میکند، سیستم آشکارسازی را مختل میسازد، کار با بعضی از جامدات فعال به مدت طولانی در دماهای بالا ممکن است منجر به تغییراتی در خواص سطحی آنها شود که احتمالا به علت از بین رفتن مواد شیمیایی جذب شده ، یا گداختن (کاهش مساحت سطح در دماهای زیر نقطه ذوب) است.
ولی چنین تغییراتی در دماهایی که در کروماتوگرافی بکار میروند غیر معمول بوده یا به وسیله عمل مقدماتی مناسبی قابل جلوگیری هستند. یک ستون پر شده از یک جامد فعال ممکن است، زمانهای بازداری خیلی بزرگتری نسبت به زمانهای بازداری حاصل در یک ستون با حجم برابر در کروماتوگرافی گاز ـ مایع تولید کند. از این رو اجسام فرارتر را میتوان به راحتی جدا کرد. حد جرم مولکولی در کروماتوگرافی گاز ـ جامد در واقع در حدود 150 است ( این نیز میتواند یک عیب به شمار آید ).
آشکارترین عیب جاذبهای جامد این است که در غلظتهای پایینتر از جسم جذب شونده غالبا همدماهای به شدت انحنادار ، از نوع همدمای لانگموپر ، تولید میکنند. این منحنیها منجر به دنبالهدار شدن و در نتیجه از بین رفتن کارایی در تجزیه به روش شستشو میشوند. بسیاری از جامدات فعال کاتالیزورهای موثری هستند، در صورتی که فعالیت کاتالیزوری در کروماتوگرافی گاز ـ مایع نادر است.
جدا سازی در دماهای بالاتر از نقطه جوش نمونه انجام میگیرد. بطوری که بسیاری از جداسازیهای انجام شده بوسیله کروماتوگرافی گاز ـ جامد روی مواد زود جوش صورت میگیرد.
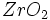 هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.
هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.عناوین یادداشتهای وبلاگ